Étude comparative in vitro de la survie des capsules probiotiques dans un environnement gastrique simulé
Résumé
Trois probiotiques commerciaux contenant principalement les espèces Lactobacillus et Bifidobacterium ont été étudiés. Ils ont été identifiés en tant que P15, P50, et P11. Les trois produits sont encapsulés dans des capsules de source végétale, avec P11 étant revêtu d’un enrobage entérique. L’objectif de cette étude était d’évaluer la désintégration des capsules et la survie microbienne des souches probiotiques lors d’une exposition à des conditions gastriques simulées. La désintégration des capsules a été effectuée en respectant le protocole de la pharmacopée des États-Unis.
Les échantillons probiotiques ont été incubés pendant les périodes de temps définies dans un environnement gastrique simulé, puis neutralisés et déposés sur un milieu de culture approprié. Après 60 minutes, les résultats ont démontré que les capsules de probiotiques à enrobage entérique protègent davantage la survie des microorganismes contre l’acide gastrique.
Introduction
Les probiotiques des genres Lactobacillus et Bifidobacterium ont le potentiel d’apporter des bienfaits de santé et thérapeutiques chez les humains (Kailasapathy et Chin, 2000). Ces bienfaits incluent (i) le renforcement de la réponse immunitaire, (ii) la prévention de maladies diarrhéiques, (iii) la prévention de l’hypercholestérolémie, (iv) l’amélioration de l’utilisation du lactose, (v) la prévention des maladies des voies gastrointestinales supérieures, et (vi) la stabilisation de la barrière que représente la muqueuse intestinale (Kailasapathy et Chin, 2000). Pour maximiser ces bienfaits, les probiotiques doivent résister à la dégradation par les enzymes digestives, être résistantes à l’action des sels biliaires, et survivre aux conditions de l’acidité gastrique (Kailasapathy et Chin, 2000). L’industrie des suppléments emploie différents types de capsules avec ou sans enrobage entérique. L’objectif de cette étude était d’évaluer la désintégration de la capsule et la survie microbienne des souches probiotiques lors de l’exposition au liquide gastrique simulé (LGS).
Matériaux et méthodologie
Échantillons d’essai et microorganismes
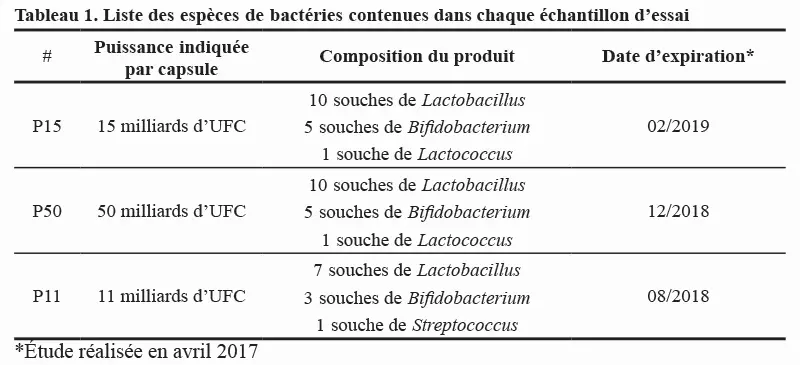
Trois produits probiotiques commerciaux ont été sélectionnés pour cette étude. Les produits sont résumés ci-dessous.
Simulation des conditions gastriques et test de désintégration
Les conditions gastriques ont été recréées en préparant un liquide gastrique simulé (LGS). Le pH de la solution était de 1,2. Six capsules par produit ont été incubées dans cette solution pendant 30 min et 60 min. Le test de désintégration a été effectué en respectant le protocole de la pharmacopée des États-Unis.
Résultats et discussion
Test de désintégration
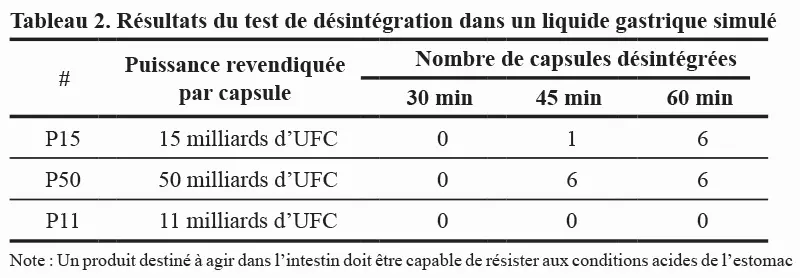
À 30 min, toutes les capsules, tous fabricants confondus, résistèrent aux conditions acides. Le P15 a commencé à se désintégrer à 45 min avec une capsule, et s’est complètement désintégré à 60 min. En ce qui concerne le P50, les six capsules se sont désintégrées à 45 min. Toutes les capsules de P11 ont résisté à la désintégration à la fin de la période de 60 minutes dans le LGS. Cela pourrait être expliqué par le revêtement entérique, qui agit en protégeant son contenu avant d’atteindre l’intestin grêle.
Les résultats présentés dans le Tableau 2 suggèrent que les produits P15 et P50 peuvent être exposés à des conditions acides qui affectent la viabilité des probiotiques qu’ils contiennent. Des études ont démontré que le temps moyen d’exposition des aliments, y compris les médicaments, à l’action du liquide gastrique est de plus de 60 minutes (Camilleri et autres, 1989).
Résistance au fluide gastrique artificiel
L’effet de l’exposition à un liquide gastrique simulé a été testé à 30 min et 60 min. Les résultats de cette étude comparative sont présentés dans le Tableau 3. D’autre part, la Figure 1 montre le pourcentage de réduction du nombre total de probiotiques par rapport au nombre initial dans les trois produits testés.

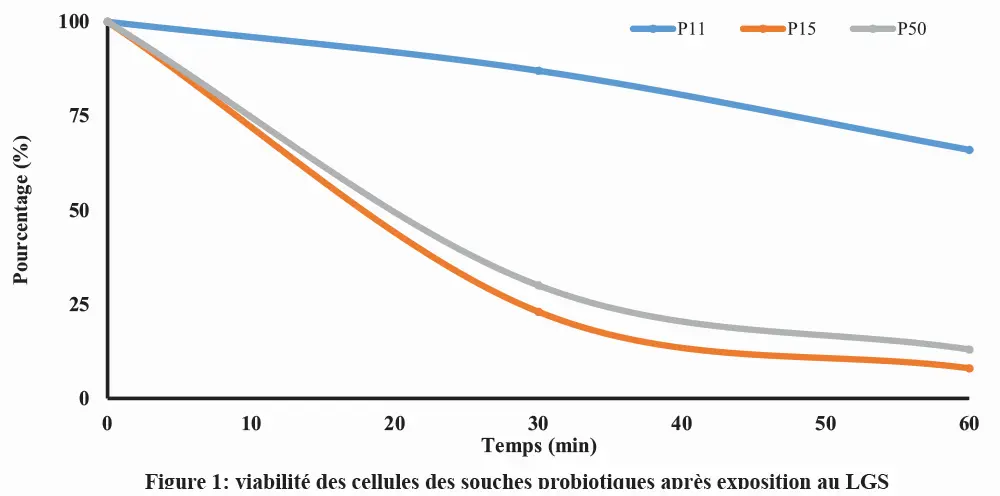
Ces illustrations mettent en évidence l’impact des conditions acides sur les probiotiques. P15 et P50 ont présenté 8 % et 13 % respectivement des cellules viables, par rapport à 66 % pour P11 (Fig. 1) après 60 min d’incubation. Après 30 min, cette viabilité a été calculée comme étant de 23 %, 30 %, et 87 % pour P15, P50, et P11, respectivement. Ces résultats démontrent que les espèces Lactobacillus et Bifidobacterium sont sensibles aux conditions acides. Ces bactéries peuplent l’intestin humain, où le pH est compris entre 6 et 7,5, selon la section de l’intestin (Maurer, J.M. et al, 2015). Ceci souligne l’importance critique de l’enrobage entérique pour un dosage à libération graduelle.
Le taux élevé de perte observé pour P15 et P50 pourrait expliquer le surdosage considérable lors de la production (473 % et 312 % pour P15 et P50, respectivement). Néanmoins, ce surdosage semble insuffisant, car seulement 40 % environ du nombre de cellules indiquées sur l’emballage restent viables après 60 min dans le liquide gastrique simulé. En revanche, P11, avec une surdose minimale de 182 %, dépassait toujours le nombre de cellules promises, avec 118 % de survie des cellules viables.
Conclusions
Les conditions acides de l’environnement gastrique sont difficiles et nuisibles à la plupart des souches probiotiques. Comme cette étude le démontre, la survie des bactéries probiotiques dans des conditions acides dépend fortement de la survie des capsules aux conditions gastriques hostiles. Les capsules sans enrobage entérique ont démontré une faible efficacité, tandis que les capsules à enrobage entérique ont démontré une viabilité plus élevée. Cela a été déterminé par les données de désintégration et les données d’énumération après exposition au LGS.
Références
Camilleri, M., et autres. « Human gastric emptying and colonic filling of solids characterized by a new method. » American Journal of Physiology-Gastrointestinal and Liver Physiology. Vol. 257, N° 2 (1989): G284–G290.
Kailasapathy, K., et J. Chin. « Survival and therapeutic potential of probiotic organisms with reference to Lactobacillus acidophilus and Bifidobacterium spp. » Immunology and Cell Biology. Vol. 78, N° 1 (2000): 80–88.
Maurer, J.M. et al. « Gastrointestinal pH and Transit Time Profiling in Healthy Volunteers Using the IntelliCap System Confirms Ileo-Colonic Release of ColoPulse Tablets. » PLoS ONE Vol. 10, N° 7 (2015): e0129076.